
Dalam kimia organik , gugus karbonil adalah sebuah gugus fungsi yang terdiri dari sebuah atom karbon yang berikatan rangkap dengan sebuah atom oksigen : C=O.
Istilah karbonil juga dapat merujuk pada karbon monoksida sebagai sebuah ligan pada senyawa anorganik atau kompleks organologam (misalnya nikel karbonil ); dalam situasi ini, karbon berikatan rangkap tiga dengan oksigen C≡O.
Senyawa karbonil
Sebuah gugus karbonil dikarakterisasikan oleh jenis-jenis senyawa berikut ini:
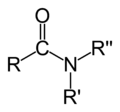
| Senyawa | Aldehida | Keton | Asam karboksilat | Ester | Amida | Enon | Asil klorida | Anhidrida asam |
| Struktur |
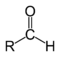
|

|
|
|
|

|

|
|
| Rumus umum | RCHO | RCOR' | RCOOH | RCOOR' | RCONR'R'' | RC(O)C(R')CR''R''' | RCOCl | (RCO) 2 O |
Senyawa karbonil lainnya termasuk urea dan karbamat . Contoh dari senyawa karbonil anorganik adalah karbon dioksida , , dan fosgena .
Reaktivitas
Oksigen lebih elektronegatif daripada karbon, sehingga rapatan elektron akan tertarik dari karbon dan meningkatkan ikatan. Oleh karena itu, karbon karbonil bersifat , sehingga lebih reaktif terhadap nukleofil . Selain itu, oksigen yang elektronegatif juga dapat bereaksi dengan elektrofil.
pada senyawa karbonil lebih asam (~10 30 kali lebih asama) daripada ikatan CH yang biasa. Sebagai contoh, nilai pK a asetaldehida dan aseton adalah 16,7 dan 19, berturut-turut. [ 1 ]
Amida adalah penggandengan ( coupling ) karbonil yang paling stabil oleh karena stabilisasi resonansinya yang tinggi di antara ikatan Nitrogen-Karbon dengan Karbon-Oksigen.
Gugus karbonil dapat direduksi oleh reagen hidrida seperti NaBH 4 dan LiAlH 4 , dan oleh reagen organologam seperti dan .
Reaksi-reaksi penting lainnya meliputi:
- Reduksi Wolff-Kishner
- Reduksi Clemmensen
- Konversi menjadi tioasetal
- Hidrasi menjadi dan , kemudian menjadi dan
- Reaksi dengan ammonia dan amina primer membentuk imina
- Reaksi dengan hidroksilamina membentuk
- Reaksi dengan anion sianida membentuk
- Oksidasi dengan oksaziridina menjadi
- Reaksi dengan dan menjadi alkena
- Reaksi Perkin
- Reaksi Cannizzaro
Senyawa karbonil α,β-takjenuh
Senyawa karbonil α,β-takjenuh adalah sebuah kelompok senyawa karbonil yang penting dengan struktur umumnya C β =C α −C=O. Pada senyawa-senyawa ini, gugus karbonil ber konjugasi dengan sebuah alkena . Hal ini menyebabkan sifat-sifat khusus senyawa ini. Sebagai contoh senyawa ini adalah akrolein , , asam akrilat , dan asam maleat . Karbonil takjenuh dapat dibuat dalam laboratorium menggunakan reaksi aldol dan reaksi Perkin .
Gugus karbonil, baik pada aldehida , asam , ataupun keton , menarik elektron dari alkena dan gugus alkena pada karbonil takjenuh, sehingga menurunkan reaktivitas terhadap elektrofil seperti bromin atau asam klorida . Sebagai kaidah umum, hidrogen melekatkan dirinya pada posisi alfa pada sebuah adisi elektrofilik . Sebaliknya, senyawa ini reaktif terhadap nukleofil pada .
Spektroskopi
- Spektroskopi inframerah : ikatan rangkap C=O menyerap sinar inframerah pada bilangan gelombang kira-kira 1600–1900 cm −1 . Lokasi persis penyerapan bergantung pada geometri molekul. Penyerapan ini dikenal sebagai "regangan karbonil". [ 2 ]
- : ikatan rangkap C=O menunjukkan resonansi yang berbeda-beda tergantung pada atom-atom tetangga, umumnya berada pada pegeseran medan bawah ( downfield shift ). NMR 13 C karbon karbonil berada pada kisaran 160-220 ppm.
Lihat pula
Referensi
- ^ Ouellette, R.J. and Rawn, J.D. “Organic Chemistry” 1st Ed. Prentice-Hall, Inc., 1996: New Jersey. ISBN 0-02-390171-3 .
- ^ Mayo D.W., Miller F.A and Hannah R.W “Course Notes On The Interpretation of Infrared and Raman Spectra” 1st Ed. John Wiley & Sons Inc, 2004: New Jersey. ISBN 0-471-24823-1 .
Pustaka tambahan
- L.G. Wade, Jr. Organic Chemistry, 5th ed. Prentice Hall , 2002. ISBN 0-13-033832-X
- The Frostburg State University Chemistry Department. Organic Chemistry Help (2000).
- Advanced Chemistry Development, Inc. IUPAC Nomenclature of Organic Chemistry (1997).
- William Reusch. VirtualText of Organic Chemistry (2004).
- Purdue Chemistry Department [1] (retrieved Sep 2006). Includes water solubility data.
- William Reusch. (2004) Aldehydes and Ketones Diarsipkan 2010-04-30 di Wayback Machine . Retrieved 23 May 2005.
- ILPI. (2005) The MSDS Hyperglossary- Anhydride .